Russian Federation
Russian Federation
Russian Federation
Russian Federation
UDC 574.24
UDC 574.632
UDC 579.68
UDC 581.1
The article presents the results of experiments on the ability of the green alga Ulva lactuca to absorb and transform diesel fuel from marine water for 5 and 10 days. The original marine water contained 0.62 mg/L of petroleum hydrocarbons, which is about 12 maximum permissible concentrations (MPC). During the experiment with the addition of 20 mg/L of diesel fuel (400 MPC) to the water, the absorption of the introduced hydrocarbons was observed in the experimental tanks without algae. Apparently, they were absorbed by water microorganisms. On the 5th day of the experiment, the petroleum hydrocarbons concentration in the water decreased by 40 % and amounted to 12 mg/L (240 MPC). When ulva thalli were added to the water, the total content of petroleum hydrocarbons in the water on the 5th day decreased by 86 % (to 2.8 mg/L), and on the 10th day, it increased (to 4.2 mg/L). A slight increase in the concentration of diesel fuel hydrocarbons in water indicates a reverse process of releasing hydrocarbons absorbed by ulva into water. In the experiment with the addition of diesel fuel to the water at a concentration of 10 mg/L, the content of hydrocarbons in algae tissues on the 5th and 10th days was recorded at the level of 0.6 mg/g. The marker ratio of Σn-alkanes / Σ petroleum products in ulva during the experiment was 0.2. A decrease in this indicator to 0.18 on the 10th day of the experiment indicates the beginning of the transformation of the hydrocarbons chemical structure. When 20 mg/L of diesel fuel (400 MPC) were added to the water, this indicator on the 5th and 10th days was 0.25 and 0.28, respectively, indicating an active process of hydrocarbon absorption by the algae surface, which was not yet complete by the 10th day. The experiment results allow us to conclude that U. lactuca is able to absorb and transform petroleum hydrocarbons and participates in the bioremediation of coastal waters.
Ulva lactuca, Barents Sea, diesel fuel, petroleum product accumulation, petroleum product destruction, pollution tolerance
Введение
В последние годы возрос интерес к возможной роли водорослей-макрофитов в биоремедиации прибрежных акваторий от нефтепродуктов (НП). Это вызвано полученными сведениями о способности водорослей не только аккумулировать НП на поверхности таллома, но и поглощать, а в дальнейшем трансформировать и включать НП в метаболизм клеток. Описываемые процессы осуществляются во многом благодаря углеводородокисляющим бактериям (УОБ), которые в большом количестве присутствуют на поверхности макроводорослей, особенно в загрязненных нефтепродуктами прибрежных акваториях [1, 2]. Объектами исследований влияния НП на водоросли, а также роли водорослей в биоремедиации среды обитания были преимущественно представители бурых водорослей: ламинариевые и фукусовые, составляющие основную фитомассу в прибрежье Баренцева моря [3, 4]. Гораздо меньше данных по указанной выше тематике было получено для зеленых водорослей, хотя, судя по имеющимся в литературе сведениям, они также обладают определенной устойчивостью к нефтяному загрязнению [5–7]. Ранее в наших экспериментах по влиянию дизельного топлива (ДТ) на ранние стадии развития Ulva lactuca было показано, что при содержании в воде ДТ в концентрации 5 мг/л (100 ПДК) наблюдается замедление развития проростков на 20-е сутки эксперимента, при 25 мг/л (500 ПДК) – на 10-е сутки, а при содержании токсиканта 50 мг/л (1000 ПДК) гибель проростков наблюдалась на 5-е сутки опыта [8]. В опытах по влиянию ДТ на близкий к Ulva lactuca вид U. intestinalis было отмечено, что добавление в среду ДТ в концентрации 1–5 мг/л (20–100 ПДК) не приводит к гибели водорослей, однако вызывает снижение фотосинтетической активности и содержания фотосинтетических пигментов. Добавление же в среду ДТ от 50 до 150 мг/л (1000–3000 ПДК) вызывает постепенные необратимые изменения у водорослей, приводящие к гибели растений, причем при содержании в воде ДТ 150 мг/л гибель происходит через 3 сут эксперимента [9]. На сегодняшний день в литературе отсутствуют сведения о диапазоне толерантности «взрослых» талломов Ulva lactuca к ДТ и способности Ulva lactuca поглощать и трансформировать токсикант.
Ulva lactuca – вид зеленых водорослей, космополит, сравнительно недавно редко встречавшийся в Баренцевом море, в настоящее время активно распространяется на литорали Восточного Мурмана [10]. Дизельное топливо является одним из самых распространенных токсикантов морских акваторий в связи с тем, что используется морским транспортом, а также отопительными береговыми комплексами (ТЭЦ) [11].
Целью нашего исследования является получение сведений о поглощении и трансформации НП тканями U. lactuca, об изменениях у водорослей, происходящих на клеточном уровне, при содержании ДТ в морской воде 10 и 20 мг/л, а также возможной роли U. lactuca в биоремедиации. В статье использованы материалы тезисов Беломорской студенческой научной сессии СПбГУ) .
Материал и методы
Талломы Ulva lactuca без признаков размножения и воду отбирали для исследования в августе 2023 г. на литорали губы Зеленецкой Баренцева моря в районе сезонной биостанции ММБИ РАН (69°07′09″ с. ш., 36°05′35″ в. д.). Эксперименты проводили в термостатируемом помещении при температуре 8–10 °С с постоянным освещением 150 мкмоль м-²с-¹, фотопериод 24L:0D (период полярного дня) и аэрацией водной среды. Воду для опытов соленостью 33 ‰ фильтровали через ватно-марлевый фильтр и охлаждали до температуры 8–10 °С. В экспериментальные сосуды в количестве 18 шт. (три – контрольных с водорослями, три – контрольных без водорослей, шесть – опытных с водорослями и шесть – без водорослей (по три на каждую концентрацию)) с подготовленной водой объемом 2 л добавляли летнее дизельное топливо в количестве 10 и 20 мг/л (200 и 400 ПДК соответственно). В сосуды, где должны были находиться водоросли, помещали взрослые талломы U. lactuca весом 5 г каждый из расчета три экземпляра на одну экспериментальную емкость. Каждый сосуд аэрировали с помощью воздушного компрессора.
Все экспериментальные емкости плотно закрывали крышкой с целью исключения потери летучих фракций ДТ. Концентрации ДТ были выбраны в целях определения толерантности к токсиканту и анализа морфологических изменений у U. lactuca. В начале (0 суток), на 5-е и 10-е сутки эксперимента образцы водорослей отбирали и исследовали методом газовой хроматографии/масс-спектрометрии на содержание в них НП. Водоросли, не подвергавшиеся воздействию НП, изучали на протяжении опыта как контрольный образец. Воду на содержание ДТ анализировали в исходном варианте, контроле и после добавления ДТ в присутствии в воде водорослей и без них. Каждый анализ воды и водорослей проходил в трех повторностях. Процесс пробоподготовки и инструментального анализа осуществляли на основе методики ЕРА 8270, подробно описанной в предыдущих исследованиях [12]. Для анализа изменений у водорослей под влиянием НП, происходящих на клеточном уровне, из талломов делали высечки 1 см2, которые помещали в пробирки Эппендорфа с фиксатором. Предфиксацию проводили 2.5%-ным глютаровым альдегидом на какодилатном буфере (к-к-б) с введением в состав фиксатора
1.5%-ного танина, а постфиксацию – 1%-ным OsO4 (оксидом осмия (VIII)) на аналогичном буфере. Осмотическое давление обоих фиксаторов доводили до осмотического давления морской воды в среде обитания (1100 мосм) с помощью сахарозы. Фиксация проходила при температуре 0…+5 °С по схеме:
предфиксация глютаровым альдегидом 18 ч, отмывка к-к-б – две смены по 6 ч, постфиксация OsO4 – 18 ч. Далее материал готовили к просмотру в электронном микроскопе JEM-100C (фирмы JEOL) по общепринятым методикам .
Результаты и обсуждение
Светооптические и электронно-микроскопические наблюдения показали, что талломы U. lactuca, взятые из места обитания, где концентрация НП была 0.62 мг/л (12 ПДК), не отличались по ультраструктуре клеток от исследованных ранее талломов ульвовых водорослей, обитающих при содержании НП в воде 0.1–0.2 мг/л (2–4 ПДК), которое наблюдается в большинстве исследованных губ побережья Кольского залива, Восточного Мурмана Баренцева моря. Все отобранные талломы были жизнеспособны в контрольных условиях до конца эксперимента. Каких-либо деструктивных изменений в морфологии клеток не наблюдалось. Хлоропласты содержали одноканальные пиреноиды (литера П на рис. 1, а) преимущественно погруженного типа, выявлялось большое число гранул крахмала (литера К на рис. 1, а), что свидетельствовало об активно идущем фотосинтезе (рис. 1, а).
Это же подтверждала и ярко зеленая окраска талломов контрольного варианта, сохранявшаяся до конца опыта. Вместе с тем на срезах ульвы контрольного варианта на всех сроках опыта в строении клеток отмечалась гетерогенность: клетки различались по степени развития фотосинтетического аппарата, парциального объема запасного вещества. Надо отметить, что такая же гетерогенность отмечалась при изучении ультраструктуры клеток ульвовых в природных и экспериментальных условиях в наших более ранних исследованиях [13]. На 5-е сутки в обоих вариантах опыта с ДТ в концентрации 10 и 20 мг/л около 90 % клеток в талломах ульвы не имели признаков повреждения, талломы сохраняли однородную зеленую окраску. Однако если в контрольном варианте и варианте с введенным ДТ в концентрации 10 мг/л пиреноиды присутствовали в большинстве хлоропластов, то при воздействии ДТ в концентрации 20 мг/л пиреноиды выявлялись лишь в хлоропластах у 30–40 % клеток (рис. 1, b), что может свидетельствовать об уменьшении активности функционирования фотосинтетического аппарата у большинства клеток ульвы. На 10-е сутки эксперимента при введенном в воду ДТ (10 мг/л) в строении большинства клеток таллома (до 70 %) по-прежнему не отмечалось каких-либо изменений. Однако небольшая часть клеток при данной концентрации, а также основная часть клеток (до 80 %) ульвы при концентрации 20 мг/л содержала минимальное количество организованных структур: остатки цитоплазмы локализовались у оболочки, хлоропласты не выявлялись (рис. 1, d). В клетках присутствовали зерна крахмала, но в гораздо меньшем количестве, чем в клетках контрольного варианта и на предыдущем этапе (5 сут) опыта. С внешней стороны оболочки клеток выявлялось большое число бактерий (рис. 1, c, d). Вместе с тем небольшая часть клеток таллома характеризовалась неповрежденной структурой.

Рис. 1. Изменения в клетках Ulva lactuca в эксперименте: a – контроль 0 сут;
b – 5 сут эксперимента при концентрации ДТ 10 мг/л (200 ПДК); с – 5 сут эксперимента при концентрации 20 мг/л (400 ПДК) ДТ; d – 10 сут эксперимента при концентрации 20 мг/л (400 ПДК) ДТ. Условные обозначения: П – пиреноид, К – гранулы крахмала, Я – ядро. Стрелками показаны бактерии на периферии таллома
Fig. 1. Changes in Ulva lactuca cells in the experiment: a – control for 0 days; b – 5 days of the experiment at 10 mg/L (200 MPC) diesel fuel (DF); c – 5 days of the experiment at 20 mg/L (400 MPC) DF; d – 10 days of the experiment at 20 mg/L (400 MPC) DF. Notations: П – pyrenoid, К – starch granules, Я – core. Arrows indicate bacteria on the thallus periphery
Результаты анализа образцов воды показали, что в течение эксперимента с добавлением в воду ДТ в концентрации 20 мг/л (без ульвы) происходит дест-
рукция и поглощение введенных углеводородов (УВ), по-видимому, микроорганизмами, присутствующими в воде. На пятые сутки опыта концентрация НП в воде снизилась на 40 % и составила 12 мг/л. Способность к биоремедиации у микроорганизмов отмечалась ранее в исследованиях с другими видами водорослей [1]. В случае добавления в воду образца ульвы валовое содержание НП в воде на 5-е сутки снизилось на 86 % и составило 2.8 мг/л, а на 10-е сутки немного увеличилось (до 4.2 мг/л). Некоторое увеличение концентрации НП в воде на 10-е сутки говорит об обратном процессе – высвобождении поглощенных УВ в воду, что может отражать изменение (частичное разрушение) мембранной системы клетки, наблюдаемое на электронно-микроскопических фотографиях. Подобный результат фиксировался и в более ранних исследованиях влияния углеводородов сырой нефти на зеленую водоросль Acrosiphonia arcta [14]. Значения показателя, отражающего степень трансформации углеводородов (∑н-алканов/∑НП), оставались высокими (> 0.2) на протяжении всего эксперимента, то есть процессы поглощения/высвобождения такого количества УВ (20 мг/л) проходят без существенной их трансформации. При добавке ДТ (20 мг/л) временного интервала в 10 сут, вероятно, недостаточно для наблюдения существенных изменений структуры нефтяных УВ как при участии микроводорослей, так и при участии ульвы.
Изменение концентрации алканов и валового содержания нефтепродуктов в тканях Ulva lactuca показано на рис. 2.
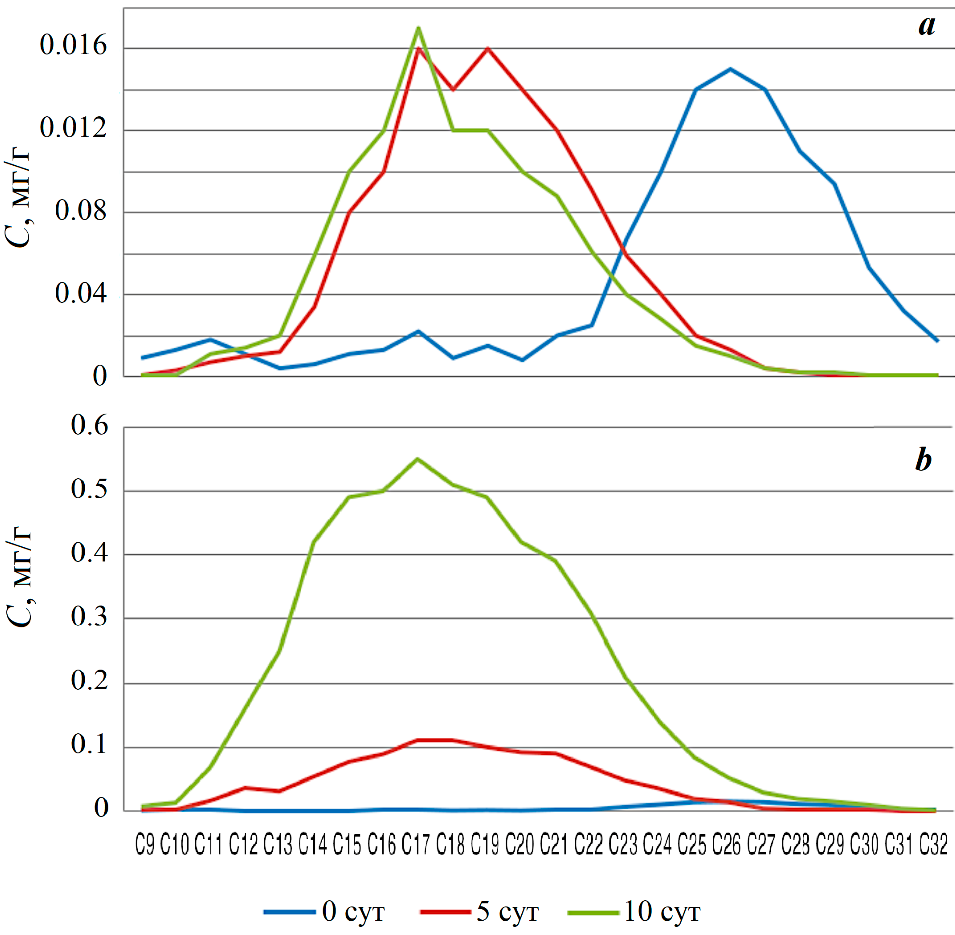
Рис. 2. Концентрация (C) н-алканов в тканях Ulva lactuca
в течение эксперимента с добавлением ДТ: а – 10 мг/л (200 ПДК); b – 20 мг/л (400 ПДК)
Fig. 2. Mass fraction of n-alkanes in the tissues of the Ulva lactuca during the experiment with the addition of DF: а – 10 mg/L (200 MPC); b – 20 mg/L (400 MPC)
Изначально образец водоросли (контроль, 0 сут) содержал 0.540 мг/г НП, из них н-алканов в диапазоне С9–С30 – 0.1 мг/г. Образец отличался повышенным для «чистых» водорослей содержанием нефтяных УВ в области С23–С30 (рис. 2). Важно отметить отсутствие у ульвы каких-либо выраженных эндогенных н-алканов по сравнению с водорослями, обитающими в загрязненных акваториях [15, 16]. На 5-е сутки эксперимента без добавления ДТ (контроль, 5 сут) валовое содержание УВ в тканях ульвы снизилось до 0.49 мг/г, на 10-е сут-
ки – до 0.34 мг/г. Уменьшилось в четыре раза и количество н-алканов в тканях водорослей – от 0.1 мкг/г (0 сут) до 0.026 мг/г (10 сут). Значение маркерного показателя ∑н-алканов/∑НП также существенно снизилось с 0.19 (в первые сутки) до 0.08 (на 5-й и 10-й день), что указывает на активную трансформацию УВ в первые пять суток. Значение данного показателя на уровне менее 0.1 характерно для водорослей, произрастающих в относительно чистых акваториях. При добавлении ДТ начинается процесс поглощения нефтяных УВ поверхностью водоросли. В опыте с добавлением ДТ в концентрации 10 мг/л содержание НП в тканях ульвы на 5-е и 10-е сутки было зарегистрировано на уровне 0.6 мг/г (рис. 2, а). Маркерное соотношение ∑н-алканов/∑НП в течение эксперимента находилось на уровне 0.2. Небольшое снижение этого показателя до 0.18 на 10-е сутки свидетельствует о начале трансформации химической структуры углеводородов. В образце ульвы, где ДТ было добавлено в количестве 20 мг/л, этот показатель на 5-е и на 10-е сутки зарегистрирован на уровне 0.25 и 0.28 соответственно, что указывает на активный процесс поглощения углеводородов, который на 10-е сутки еще не завершился. При добавлении 20 мг/л максимум содержания НП в водоросли был зарегистрирован на 10-е сутки эксперимента и составил 18 мг/г (рис. 2, b).
Обобщенные результаты эксперимента с Ulva lactuca показаны в таблице.
Процессы поглощения и трансформации НП характерны для ульвы так же, как и для всех ранее изученных видов водорослей-макрофитов [12, 14]. По сравнению с другой зеленой водорослью – акросифонией [14] – ульва демонстрирует более высокую скорость поглощения/трансформации УВ, что может быть обусловлено различием в строении таллома: пластинчатым у ульвы и сифоновым у акросифонии. Можно предположить, что пластинчатое строение таллома более благоприятно для расположения эпифитных углеводород-окисляющих бактерий.
Валовое содержание НУ в воде (мг/л) и в водорослях (мг/г) в ходе эксперимента при добавлении 20 мг/л (400 ПДК) ДТ
Gross content of petroleum hydrocarbons (PH) in water (mg/L) and in algae (mg/g) during the experiment with the addition of 20 mg/L (400 MPC) DF
|
Время, сут / |
НУ в воде / |
НУ в водорослях / |
|
0 |
20 |
0.54 |
|
5 |
2.8 |
4 |
|
10 |
4.2 |
18 |
Заключение
Проведенные опыты продемонстрировали, что воздействие летнего ДТ в концентрации 10 мг/л (200 ПДК) в течение 10 сут и в концентрации 20 мг/л (400 ПДК) в течение 5 сут при температуре 8–10 °С не является летальным для литорального вида зеленых водорослей Ulva lactuca. По-видимому, длительное произрастание в природных условиях при концентрации НП около 0.6 мг/л (12 ПДК) позволяет клеткам ульвы выработать адаптивные реакции, выдерживать разовые выбросы (утечки) НП. Показано, что U. lactuca при загрязнении ДТ морской воды достаточно быстро включается в биоремедиацию, аккумулируя, поглощая и активно трансформируя нефтепродукты. На основании данного эксперимента, а также литературных данных можно предположить, что относительно широкий диапазон толерантности к нефтепродуктам является одним из факторов, позволившим U. lactuca занять определенную экологическую нишу на литорали Мурманского побережья Баренцева моря, богатого в настоящее время источниками нефтяного загрязнения.
1. Bakterii-epifity buryh vodorosley v utilizacii nefti v ekosistemah severnyh morey / E. B. Semenova [i dr.] // Vestnik Moskovskogo universiteta. Seriya 16. Biologiya. 2009. № 3. S. 18–22. EDN KYQLET
2. Pugovkin D. V., Liaimer A., Jensen J. B. Epiphytic bacterial communities of the alga Fucus vesiculosus in oil-contaminated water areas of the Barents Sea // Doklady Bio-logical Sciences. 2016. Vol. 471. R. 269–271. https://doi.org/10.1134/S0012496616060053
3. Malavenda S. V., Shoshina E. V., Kapkov V. I. Vidovoe raznoobrazie makrovodorosley v razlichnyh rayonah Barenceva morya // Vestnik MGTU. 2017. T. 20, № 2. S. 336–351. EDN ZCHVMH. https://doi.org/10.21443/1560-9278-2017-20-2-336-351
4. Wrabel M. L., Peckol P. Effects of bioremediation on toxicity and chemical composi-tion of No. 2 Fuel Oil: Growth responses of the brown alga Fucus vesiculosus // Marine Pollution Bulletin. 2000. Vol. 40, iss. 2. P. 135–139. https://doi.org/10.1016/S0025-326X(99)00181-2
5. Toxic effect of oil spill on the growth of Ulva pertusa by stable isotope analysis / Y. X. Liu [et al.] // IOP Conference Series: Earth and Environmental Science. The 5th International Conference on Water Resource and Environment (WRE 2019), 16–19 July 2019, Macao, China. IOP Publishing, 2019. Vol. 344. 012062. https://doi.org/10.1088/1755-1315/344/1/012062
6. In vitro exposure of Ulva lactuca Linnaeus (Chlorophyta) to gasoline–Biochemical and morphological alterations / F. K Pilatti [et al.] // Chemosphere. 2016. Vol. 156. P. 428–437. https://doi.org /10.1016/j.chemosphere.2016.04.126
7. El Maghraby D., Hassan I. Photosynthetic and biochemical response of Ulva lactuca to marine pollution by polyaromatic hydrocarbons (PAHs) collected from different re-gions in Alexandria City, Egypt // Egyptian Journal of Botany. 2021. Vol. 61, iss. 2. P. 467–478. https://doi.org/10.21608/ejbo.2021.37571.1531
8. Salahov D. O., Voskoboynikov G. M., Ryzhik I. V. Vliyanie dizel'nogo topliva na razvitie prorostkov Ulva lactuca (Chlorophyta) Barenceva morya // Nauka Yuga Rossii. 2020. T. 16, № 1. S. 55–59. EDN BMEVGF. https://doi.org/10.7868/S25000640200107
9. The changes in the morpho-functional state of the green alga Ulva intestinalis L. in the Barents Sea under the influence of diesel fuel / D. O. Salakhov [et al.] // IOP Conference Series: Earth and Environmental Science. IOP Publishing, 2021. Vol. 937, iss. 2. 022059. https://doi.org/10.1088/1755-1315/937/2/022059
10. Occurrence of Ulva lactuca L. 1753 (Ulvaceae, Chlorophyta) at the Murman Soast of the Barents Sea / S. V. Malavenda [et al.] // Polar Research. 2018. Vol. 37. 1503912. https://doi.org/10.1080/17518369.2018.1503912
11. Patin S. A. Neftyanye razlivy i ih vozdeystvie na morskuyu sredu i bioresur-sy. Moskva : Izd-vo VNIRO, 2008. 508 s. URL: http://hdl.handle.net/123456789/1264 (data obrascheniya: 23.11.2024).
12. Pogloschenie i preobrazovanie dizel'nogo topliva vodorosl'yu Palmaria palmata (Linnaeus) F. Weber et D. Mohr, 1805 (Rhodophyta) i ee vozmozhnaya rol' v bioremediacii morskoy vody / G. M. Voskoboynikov [i dr.] // Biologiya morya. 2020. T. 46, № 2. S. 135–141. EDN THCPKE. https://doi.org/10.31857/S0134347520020102
13. Voskoboynikov G. M., Kamnev A. N. Morfofunkcional'nye izmeneniya hloropla-stov v ontogeneze vodorosley. Sankt-Peterburg : Nauka, 1991. 95 s.
14. Vliyanie syroy nefti na simbioticheskuyu associaciyu zelenoy vodorosli Acrosiphonia arcta (Dillwyn) Gain i epifitnyh bakteriy / G. M. Voskoboynikov [i dr.] // Morskoy biologicheskiy zhurnal. 2023. T. 8, № 1. S. 16–26. EDN LHMCGS. https://doi.org/10.21072/mbj.2023.08.1.02
15. Mironov O. G. Vzaimodeystvie morskih organizmov s neftyanymi uglevodoroda-mi. Leningrad : Gidrometeoizdat, 1985. 127 s.
16. Oil pollution of marine algae / N. Binark [et al.] // Bulletin of Environmental Contami-nation and Toxicology. 2000. Vol. 64. P. 866–872. https://doi.org/10.1007/s001280000083